


當下我國正處于新型冠狀病毒2019-nCoV疫情發展階段,該病毒感染主要會造成的新型的急性肺炎癥狀(WHO已將其名為NCOVID19),疫情已在全國范圍內肆虐超過20天,對我國民生健康和經濟造成極大影響。目前網上涌現多篇關于新型冠狀病毒2019-nCoV實驗室檢測技術的文章,文章質量水平千差萬別,良莠不齊,同時由于針對新型冠狀病毒2019-nCoV的實驗室檢測技術手段受到了全國人民前所未有的關注,部分虛假、過度、錯誤的宣傳文章對廣泛民眾產生了誤導,甚至造成恐慌。因此,為正面宣傳新型冠狀病毒2019-nCoV相關的實驗室檢測技術,使普通民眾科學地理解新型冠狀病毒2019-nCoV的診斷與防控知識,引導正確的觀點走向,現根據國家各部門頒發的相關指南共識對新型冠狀病毒2019-nCoV感染肺炎病例的實驗室檢測技術進行整理和科普。
醫學實驗室檢測是指以提供人類疾病診斷、管理、預防和治療或健康評估的相關信息為目的,對來自人體的標本進行臨床檢驗,其中包含臨床血液與體液檢驗、臨床化學檢驗、臨床免疫檢驗、臨床微生物檢驗、臨床細胞分子遺傳學檢驗等內容,針對病毒類感染病例主要進行血液學檢查和呼吸道病原學檢測。
病毒感染相關的血液學檢查主要包括血常規、血生化以及其他針對性的檢測項目,相關指標為臨床常用的病毒感染診斷指標,為疾病的輔助診斷提供依據。
1、血常規
血常規中的許多項具體指標都是一些常用的敏感指標,對機體內許多病理改變都有敏感反映,其中又以白細胞計數、紅細胞計數、血紅蛋白和血小板最具有診斷參考價值,許多患者在病因不明時可以做血常規檢查對其進行輔助診斷。此外,血常規檢查還是觀察治療效果、用藥或停藥、繼續治療或停止治療、疾病復發或痊愈的常用指標。

NCOVID19肺炎發病初期白細胞總數大部分降低或正常,淋巴細胞計數減少,單核細胞增加或正常。淋巴細胞絕對值如果小于0.8×109/L,一般建議3 d后復查血液常規變化。根據鐘南山院士的最新研究發現82.1%的患者淋巴細胞減少、36.2%的患者血小板減少,總體患者中觀察到白細胞減少的比例約占33.7%,嚴重病例白細胞、淋巴細胞減少、血小板減少明顯。
2、血生化:肝酶、心肌酶、乳酸脫氫酶、肌紅蛋白、肌鈣蛋白
血生化是檢測存在于血液中的各種離子、糖類、脂類、蛋白質以及各種酶、激素和機體的多種代謝產物的含量,可以為醫生提供診斷與治療依據,并能幫助臨床確定病情、監測治療效果。

NCOVID19肺炎部分患者出現肝酶、心肌酶、乳酸脫氫酶、血沉和肌紅蛋白增高,部分危重者可見肌鈣蛋白增高。
3、其他檢測項目:C反應蛋白(CRP)、降鈣素原(PCT)、D-二聚體、血沉、凝血像、血氣分析、乳酸等
針對感染性疾病臨床上常采用各種針對性的檢測項目進行輔助診斷,為醫生提供診斷與治療依據。
CRP和PCT的檢測對鑒別是否合并肺部的細菌感染有一定價值,多數NCOVID19患者CRP和血沉升高,重癥患者D-二聚體明顯升高,同時出現凝血功能的障礙,外周血管的微血栓形成。此外,血氣分析有助于判斷重癥患者的氧合情況,結合乳酸的升高可以篩查高危的氧合障礙患者
CT是用X線束對人體某部一定厚度的層面進行掃描,由探測器接收透過該層面的X線,轉變為可見光后,由光電轉換變為電信號,再經模擬/數字轉換器(analog/digitalconverter)轉為數字,輸入計算機處理。
新冠病毒CT的影像學表現與很多其他病毒性肺炎,如流感、呼吸道合胞病毒、腺病毒感染等比較類似,很難做鑒別性診斷。CT(電子計算機斷層掃描)作為臨床影像學篩查指標具有重要價值,另外無論從早期診斷、鑒別診斷、排除診斷還是最終確診等方面都還具有一定的局限性,更無法替代病原學診斷。因此,目前的技術水平下,最終的確診還是要靠試劑盒核酸檢測。
呼吸道病原學檢測是指采用醫學檢測技術手段針對進入人體的呼吸道病原體進行檢測,其目的是確定呼吸道病原體感染的發生和性質,在疾病早期提供恰當的治療方案,并采取有效的預防措施,防止感染傳播造成的危害。
呼吸道病原學檢測均為病原體的針對性檢測,醫學上在使用某種針對性檢測項目做臨床診斷時常用敏感性(Sensitivity)和特異性(Specificity)來衡量檢測項目的準確度和有效性。因此我們在這里先把敏感性和特異性的概念及其影響講清楚。
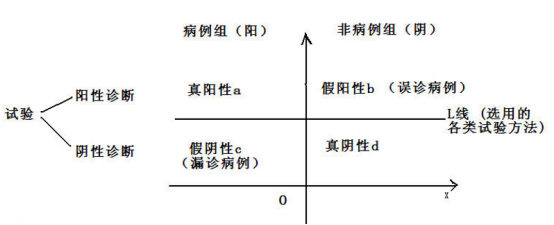
如圖所示,試驗指各類檢測項目,在評價某種檢測項目鑒別區分病例組(陽性病例)和非病例組(陰性病例)的能力時,將病例的真實情況作為橫坐標,檢測項目得出的檢測結果作為縱坐標,真實情況與檢測結果一致時檢測結果為真,不一致時檢測結果為假。由此引申出敏感性和特異性等概念如下:
A.敏感性(具有該特性的對象被預知的可能性大小)=真陽性率=a/a+c;
B.特異性(對象所具有的特殊屬性的程度)=真陰性率=d/b+d;
C.漏診率=1-敏感性=c/a+c;
D.誤診率=1-特異性=b/b+d
此外,最重要的是可以借由上圖分析敏感性與特異性的關系:
A. 高敏感性→上述a增大→L線下移,無限接近X軸→c、d越來越小,b越來越大,即低漏診率,高誤診率和低特異性(低真陰性率)。
B. 高特異性→上述d增大→L線上移,無限接近+∞→a、b越來越小,c越來越大,即高漏診率,低誤診率和低敏感性(低真陽性率)。
由此可見,高敏感性與高特異性不可兼得,高敏感性則低特異性,高特異性則低敏感性。可采用敏感性高與特異性高的不同檢測方法相結合的方式提高整體檢測的準確度。
接下來我們向大家介紹病原學檢測的各種技術方法:
1、病毒培養分離與鑒定
病毒培養一般有細胞培養和雞胚培養(9-11日齡雞胚)這兩種方法。從呼吸道標本培養分離出的病毒進行鑒定常作為呼吸道病原體實驗室診斷的金標準,其敏感性和特異性均在90%以上,但多數病毒培養比較困難,技術難度高且操作復雜,生物安全條件要求高,檢測周期長,一般不應用于臨床檢測。
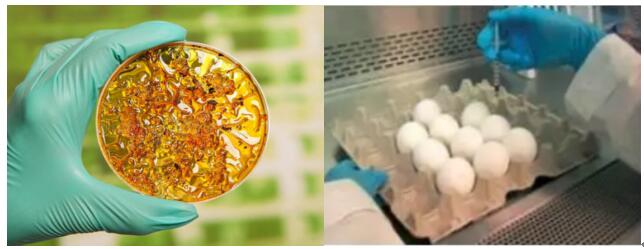
國家衛健委發布的《流行性感冒診療方案(2019年版)》指出“從呼吸道標本培養分離出流感病毒是流感診斷的金標準。但由于病毒培養周期較長,生物安全條件要求高,不建議應用于臨床診療”。無獨有偶,在目前公布的各項新型冠狀病毒2019-nCoV防治診療指南中均未把病毒培養分離與鑒定列入病原學檢測項目。
2、病毒抗原檢測
病毒的結構一般由外層的衣殼蛋白包含病毒核酸物質組成,一般來說病毒的衣殼蛋白可作為病毒抗原(Virus antigen)通過病毒抗原檢測技術被檢測到。病毒抗原檢測技術主要采用免疫層析技術,利用具有高度特異的單克隆抗體來識別呼吸道標本中的病毒抗原,待測樣本中如有相對應的抗原,與試劑板中包被的抗體結合,抗體上面標記的物質呈現顏色變化,出現對應條帶,通過觀察條帶可以得到相關的檢測結果。抗體標記物一般為膠體金、乳膠顆粒和量子點熒光納米微球等材料。這個方法在臨床應用中操作簡便,速度快,10-15分鐘就可獲得檢測結果,可以做床旁檢測。病毒感染人體后一般會經歷一段時間的“潛伏”進行病毒復制,隨后病毒大量排出引發病理反應。病毒抗原檢測標本一般為上呼吸道標本,一般采用口咽拭子或鼻咽拭子進行取樣,在發病初期具有良好的檢測效果,但隨病情的發展和治療其檢測陽性率有所下降。
目前臨床上應用最廣泛的病毒抗原快速檢測技術是針對流行性感冒的檢測,全國有超過10家廠家可生產針對流感病毒抗原快速檢測的試劑。流感抗原檢測的靶標一般是流感病毒NP和MP蛋白,可以確定病毒是甲型還是乙型,但無法確定病毒的亞型。流感病毒抗原檢測一般采用膠體金標記,也有采用熒光標記法進行標記的,熒光標記法會比膠體金標記的方法敏感性更高,多需相應儀器,如熒光顯微鏡,熒光檢測設備。流感病毒抗原檢測試劑的敏感性受到抗體原料和標記物性能的影響極大,使不同廠家檢測試劑的敏感性跨度較大,一般在20%-70%之間,并且在病毒載量較低時無法檢測到目標病毒,檢測陰性不能作為排除流感感染的診斷標準,各廠家流感抗原檢測試劑的特異性一般在90%以上,因此檢測陽性支持診斷。在國家衛健委發布的《流行性感冒診療方案(2019年版)》中推薦流感病毒抗原檢測可作為確診方法,但同時也提示其檢測陰性不能排除流感。抗原檢測方法因其快速方便,特異性好,比較容易在各層級醫院中普及。
反觀針對新型冠狀病毒2019-nCoV抗原的檢測則尚處于前期研發階段,尚無有注冊申報的產品出來,究其主要原因應與試劑原材料有關,主要是目前尚無法獲得針對新型冠狀病毒2019-nCoV抗原蛋白特異性高的單克隆抗體。盡管早在2020年1月底就有公司聲稱獲得了新型冠狀病毒2019-nCoV抗原蛋白的抗體,至今也有數家公司宣布可對外提供相應抗體,但通過查詢相關信息并進行深入分析可得知目前可提供的新型冠狀病毒2019-nCoV抗原蛋白抗體應均為通過動物免疫獲得的多抗而并非單克隆抗體,如采用多抗作為原料生產新型冠狀病毒2019-nCoV抗原檢測試劑則會對試劑檢測結果造成極大影響。即使經過一段時間的研發和生產有公司可提供針對新型冠狀病毒2019-nCoV抗原蛋白的單克隆抗體,其作為原材料加入到抗原檢測試劑中的效果仍需要大批臨床實驗數據的驗證。然而流感病毒在全球范圍內肆虐百年,并且每年有周期性的流行,國內外能夠生產流感病毒抗原單克隆抗體的廠家超過百家,因此生產抗原檢測試劑的廠家可以獲得性能較好的單克隆抗體原材料進行研發和生產,最終獲得流感病毒抗原檢測試劑。綜上所述,新型冠狀病毒2019-nCoV抗原檢測試劑尚有很長的一段路要走,但一旦試劑研發成功并獲得國家藥監局的注冊審批則完全可以快速應用到臨床,以其操作簡單、檢測速度快、特異性高、易普及等優點會快速被各層級醫療機構廣泛接受。
3、病毒抗體檢測
抗體(Antibody)是指機體由于抗原的刺激而產生的具有保護作用的蛋白質,是一種由漿細胞(效應B細胞)分泌,被免疫系統用來鑒別與中和外來物質如細菌、病毒等的大型Y形蛋白質,僅被發現存在于脊椎動物的血液等體液中,及其B細胞的細胞膜表面。抗體是一類能與抗原特異性結合的免疫球蛋白(immunoglobulin,Ig),由四條多肽鏈組成,各肽鏈之間由數量不等的鏈間二硫鍵連接,大致可分為5類,即IgM、IgD、IgG、IgA和IgE。人體在接觸外來抗原(Antigen)的時候,最早產生的抗體是IgM,是由B細胞表面受體直接分泌,產生IgM的B細胞進入淋巴結,在發生中心接受T細胞和抗原提呈細胞的刺激,進一步成熟,分化為漿細胞,大量產生IgG。
目前臨床上針對抗體的檢測一般也采用前面抗原檢測中提到的免疫層析技術,但檢測試劑原料與抗原檢測不同,抗體檢測是利用病毒抗原蛋白來識別血液標本中的病毒由病毒感染所產生的抗體,一般針對血液中病毒特異性的IgM和IgG進行檢測。
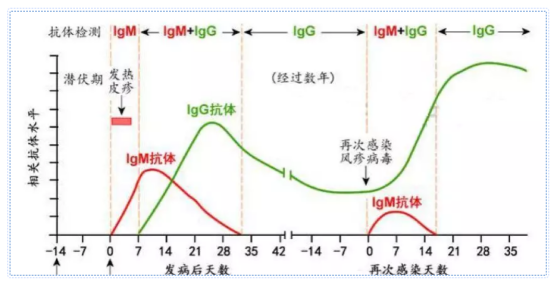
IgM是初次體液免疫應答中最早出現的抗體,IgG是血清和體液中含量最高的抗體,占血清總Ig的75%~80%,其親和力高,在體內分布廣泛。抗體檢測的方法,之前應用的比較多,但隨著我們認知的逐漸提高,在2019年的流感診療方案中已經很明確流感病毒IgG 抗體水平恢復期比急性期呈4 倍或以上升高僅有回顧性診斷意義,無法用于病毒感染的診斷,而IgM 抗體檢測敏感性較低,不建議常規使用。其實不僅是不適合流感的診斷,大多數呼吸道病毒都不需要這種抗體檢測方法,其主要原因是抗體一般在患者恢復期才大量產生,時效性差,無法作為病毒感染的早期診斷,對傳染性極高新型冠狀病毒2019-nCoV的診斷和防控毫無意義。因此,目前各項新型冠狀病毒2019-nCoV防治診療指南中均未把病毒抗體檢測列入病原學檢測項目。
4、病毒核酸檢測
所有生物除朊病毒外都含有核酸,核酸包括脫氧核糖核酸(DNA)和核糖核酸(RNA),新型冠狀病毒是一種僅含有RNA的病毒,病毒中特異性RNA序列是區分該病毒與其它病原體的標志物。新型冠狀病毒2019-nCoV出現后,我國科學家在極短的時間里完成了對新型冠狀病毒2019-nCoV全基因組序列的解析,并通過與其它物種的基因組序列對比,發現了新型冠狀病毒2019-nCoV中的特異核酸序列。臨床實驗室檢測過程中,如果能在患者樣本中檢測到新型冠狀病毒2019-nCoV的特異核酸序列,應提示該患者可能被新型冠狀病毒2019-nCoV感染。
檢測新型冠狀病毒2019-nCoV特異核酸序列的方法最常見的是熒光定量PCR(聚合酶鏈式反應)。因PCR反應模板僅為DNA,而新型冠狀病毒2019-nCoV為RNA病毒,因此在進行PCR反應前,應將新型冠狀病毒核酸(RNA)逆轉錄為DNA。在PCR反應體系中,包含一對特異性引物以及一個探針,該探針為一段特異性寡核苷酸序列,兩端分別標記了報告熒光基團和淬滅熒光基團。探針完整時,報告基團發射的熒光信號被淬滅基團吸收;如反應體系存在靶序列,PCR反應時探針與模板結合,DNA聚合酶沿模板利用酶的外切酶活性將探針酶切降解,報告基團與淬滅基團分離,發出熒光。每擴增一條DNA鏈,就有一個熒光分子產生。熒光定量PCR儀能夠監測出熒光到達預先設定閾值的循環數(Ct值)與病毒核酸濃度有關,病毒核酸濃度越高,Ct值越小。
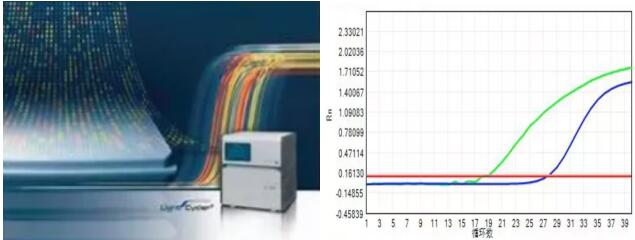
核酸檢測是分子診斷的主要技術手段,是當前臨床病原微生物診斷技術的前沿,是肺部感染診斷技術的發展方向,該方法的敏感性超過90%,特異性更是接近100%,目前已經在臨床上被廣泛用于各種呼吸道病原體的確診檢測。國家衛健委發布的《流行性感冒診療方案(2019年版)》中指出“:病毒核酸檢測的敏感性和特異性很高,且能區分病毒類型和亞型。目前主要包括實時熒光定量PCR 和快速多重PCR。熒光定量PCR 法可檢測呼吸道標本(鼻拭子、咽拭子、鼻咽或氣管抽取物、痰)中的流感病毒核酸,且可區分流感病毒亞型。” 在目前公布的各項新型冠狀病毒2019-nCoV防治診療指南中均把呼吸道或血液標本中的新型冠狀病毒2019-nCoV核酸檢測陽性定為確診方法。
但隨著新型冠狀病毒2019-nCoV核酸檢測試劑的廣泛投入使用,越來越多的問題暴露出來,其中最引人注意的是病毒核酸檢測出現過多假陰性的問題,敏感性超過90%核酸檢測試劑為何存在較多的假陰性結果,我們針對此問題也整理了相關資料并在此進行詳細描述。總體上講核酸檢測的結果受到疾病發展過程、標本采集、標本保存與運輸、核酸提取、擴增體系、檢測操作環境以及人員操作等因素的影響。
5、病原學檢測方法的選擇:
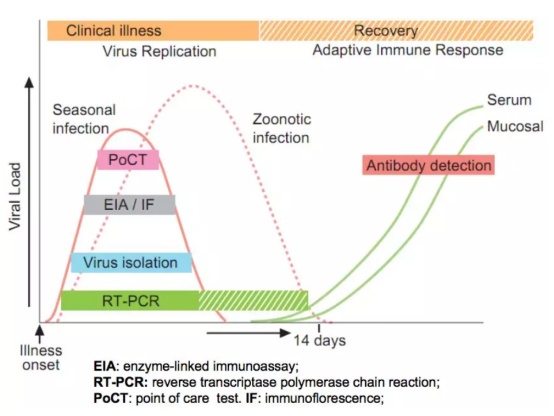
由于新型冠狀病毒2019-nCoV的臨床研究有限,因此我們參考流感檢測時間窗口明確當前新冠病毒2019-nCoV的實驗室檢測方法的選擇。根據流感檢測的時間窗口我們可以看到比如POCT、熒光檢測技術、病毒分離培養法、RT-PCR、抗體檢測等方法,它們檢測的時間和時間段有所不同,病毒抗原檢測(以POCT或熒光檢測技術開展),病毒分離培養法和核酸檢測(以RT-PCR技術開展)的檢測窗口靠前,抗體檢測滯后。呼吸道病毒診斷做抗體檢測或者培養在臨床診斷中價值不高,前者影響因素太多(如產生抗體的時間窗較長,受人體自身免疫狀況影響較大),后者很難滿足即時檢測的需求。因此在各項指南和共識中指出目前臨床上針對流感病毒的病原學檢測集中于抗原檢測和核酸檢測兩項,而針對新型冠狀病毒2019-nCoV的病原學檢測僅限于核酸檢測。
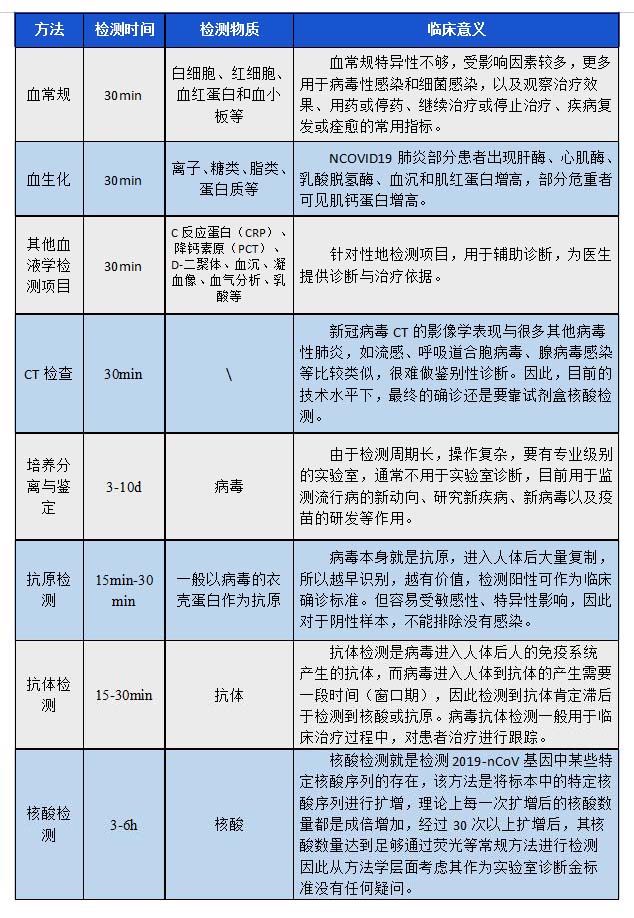
針對上文論述,我們總結了不同方法學的差異:
引用指南包括:
中華人民共和國國家衛生健康委員會發布的《新型冠狀病毒感染的肺炎診療方案(試行第五版修正版)》、《新型冠狀病毒肺炎防控方案(第四版)》、《WS 286-2008 傳染性非典型肺炎診斷標準》、《流行性感冒診療方案(2019年版)》
武漢大學中南醫院新型冠狀病毒感染的肺炎防治課題組發布的《新型冠狀病毒(2019-nCoV)感染的肺炎診療快速建議指南(標準版)》
華中科技大學同濟醫學院附屬同濟醫院救治醫療專家組發布的《新型冠狀病毒感染的肺炎診療快速指南(第三版)》
北京協和醫院發布的《關于“新型冠狀病毒感染的肺炎”診療建議方案(V2.0)》
中華醫學會兒科學分會呼吸學組呼吸道感染協作組發布的《兒童呼吸道感染微生物檢驗標本采集轉運與檢測建議(病毒篇)》
說明:主要以國家衛健委出臺的方案為準,武漢和北京醫院的方案與國家衛健委方案不沖突,作為輔助參考,鑒于新型冠狀病毒2019-nCoV屬于新型病毒,其相關的各項研究均屬于早期階段,缺少大量臨床數據支撐,故部分檢測方案數據參考國家衛健委發布的SARS肺炎診斷標準和流感診斷方案。
